长生生物问题疫苗曝光 长生生物究竟隐藏了什么真相
疫苗一直以来都是全球最主要的一种药物之一,现在的疫苗也不像很久之前一样需要花大价钱才能打。根据最新报道成长生生物问题疫苗曝光,消息出来之后引来了很多网友的热议,对于长生生物问题疫苗曝光一事,有网友提问称长生生物究竟隐藏了什么真相?
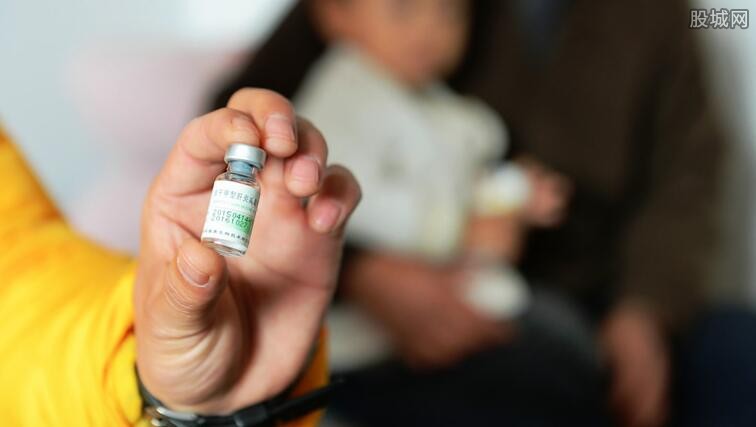
一位不具姓名的行业人士告诉《华夏时报》记者,简单来说,疫苗的采购主要由疾控中心负责,之后疫苗逐级分发到地方防疫站等疾控机构对儿童进行接种。记者查询2016年修订的《疫苗流通和预防接种管理条例》,山东省地区的百白破疫苗采购主要由省级疾控机构制定使用计划,再通过省级公共资源交易平台进行。另外根据条例,涉事企业最近几年的疫苗审批等文件、销售及接种记录,都有留存可以备查。
另外,此次长生生物子公司长春长生生产的百白破疫苗于2017年10月25日被以“劣药”立案调查,近日才收到了吉林省食药监局的行政处罚,不符合条例7日或15日的处理时限规定。
该行业人士曾撰文表示,中国各级疾控部门实际上参与到了疫苗品规遴选、疫苗采购、疫苗价格形成、疫苗配送、接种人员资质认证与监管等诸多环节中,成为中国疫苗市场的最重要的参与者之一。
根据条例,疫苗分为两类。第一类由政府免费向公民提供,第二类由公民自费并且自愿受种的其他疫苗。此次涉事的百白破疫苗和狂犬病疫苗,前者属于一类疫苗,后者属于二类疫苗。
条例规定,疫苗的采购是通过省级公共资源交易平台进行。省级疾控机构根据需要,制定本地区第一类疫苗的使用计划,并向负责采购第一类疫苗的部门报告,同时报同级人民政府卫生主管部门备案。由负责采购第一类疫苗的部门与疫苗生产企业签订政府采购合同。
第二类疫苗由省级疾控机构组织在省级公共资源交易平台集中采购,由县级疾控机构向疫苗生产企业采购后供应给当地接种单位。疫苗生产企业直接向县级疾控机构配送第二类疫苗,或者委托具备冷链储存、运输条件的企业配送。
疫苗生产企业在销售疫苗时,应当提供由药品检验机构依法签发的生物制品每批检验合格或者审核批准证明复印件,并加盖企业印章。疾控机构、接种单位在接收或者购进疫苗时,应保存至超过疫苗有效期2年备查。
按照条理规定,疾控机构应当建立真实、完整的购进、储存、分发、供应记录,做到票、账、货、款一致,并保存至超过疫苗有效期2年备查。疾控机构接收或者购进疫苗时应当索要疫苗储存、运输全过程的温度监测记录。
对不能提供全过程温度监测记录或者温度控制不符合要求的,不得接收或者购进,并应当立即向药品监督管理部门、卫生主管部门报告。实施接种的接种单位,接种记录保存时间不得少于5年疫苗生产企业也应当依照规定,建立真实、完整的销售记录,并保存至超过疫苗有效期2年备查。
疫苗在储存、运输、供应、销售、分发和使用等环节中的质量,由药品监督管理部门进行监督检查。对有证据证明可能危害人体健康的疫苗及其有关材料可以采取查封、扣押的措施,并在7日内作出处理决定;疫苗需要检验的,应当自检验报告书发出之日起15日内作出处理决定。据了解,该条例2016年修订,也与当年爆发重大疫苗造假事件有关。
另外,针对网上盛传的国家食药监总局副局长孙咸泽此前曾因“三鹿事件”被处理的说法,有观察人士撰文指出“三鹿事件”爆发时,其职务为该局食品安全协调司司长,并不对“三鹿事件”承担直接责任,因当时的食药监局没有执法权,不是食品安全监管的主要部门。
7月15日长春长生因狂犬疫苗记录造假而遭到食药监局的通报。7月18日,长春长生公告称,吉林省食药监局对其下达的处罚决定书,批次为201605014——01的百白破疫苗检验结果不合格。之后根据披露,不合格的这批百白破疫苗全部流入山东。